В этом уроке рассмотрим отличия в строении твердых тел, жидкостей и газов, объясним их свойства на основе движения и взаимодействия молекул.
Известно, что вещества могут находиться в трех агрегатных состояниях: твердом, жидком и газообразном. Твердые тела сохраняют объем и форму, жидкости меняют форму, но сохраняют объем. Газы не сохраняют ни форму, ни объем, занимают все предоставленное пространство. Почему свойства одного и того же вещества в разных состояниях различны?
Чтобы ответить на этот вопрос, вспомним, что все вещества состоят из молекул, между которыми есть межмолекулярные расстояния. Молекулы находятся в непрерывном беспорядочном движении. Отличаются ли молекулы твердых тел, жидкостей и газов?
Лед, вода и пар – это разные состояния одного и того же вещества – воды, значит, молекулы льда, воды и пара одинаковы. Это утверждение справедливо для любых веществ: молекулы одного и того же вещества одинаковы во всех состояниях.
Рассмотрим свойства газа.
Газ не сохраняет свой объем, его можно сжать. При сжатии уменьшается объем газа, значит, в газах расстояния между молекулами намного больше размеров самих молекул, следовательно, притяжение между молекулами слабое. Именно поэтому молекулы газа могут двигаться беспорядочно во всех направлениях и занимать весь предоставленный объем.
В жидкостях молекулы расположены близко друг к другу.
Расстояния между молекулами жидкости сравнимы с размерами самих молекул, и притяжение между молекулами больше, чем в газах. Молекулы жидкости не могут расходиться на большие расстояния друг от друга. Поэтому жидкости сохраняют свой объем. Но притяжение между молекулами не настолько сильное, чтобы удерживать их прочно друг около друга, и молекулы жидкости перескакивают с места на место, меняют свое положение, поэтому жидкость обладает текучестью и меняет свою форму, принимая форму сосуда. В отличие от газов, жидкости трудно сжать, так как при дальнейшем сближении молекулы начинают отталкиваться друг от друга.
В твердых телах расстояния между молекулами меньше размеров самих молекул, и притяжение между молекулами еще больше, чем в жидкостях. Молекулы твердых тел силами притяжения удерживаются в определенном положении, не могут далеко передвигаться и только колеблются около этого положения. Поэтому твердые тела сохраняют не только свой объем, но и форму.
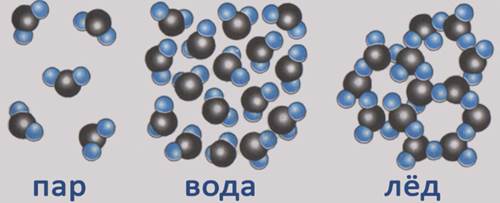
На рисунке представлено расположение молекул водяного пара, воды и льда. Из-за разного расположения молекул свойства воды в трех агрегатных состояниях различны.
Определенный порядок в расположении молекул твердого тела называют кристаллической решеткой. Такие твердые тела называют кристаллами. Это, например, лед, соль, металлы, алмаз.
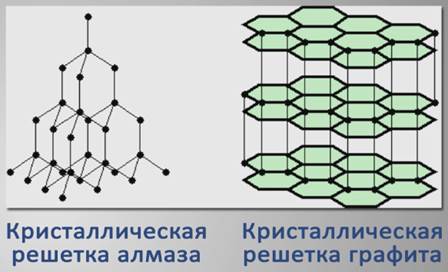
Свойства твердых тел зависят от вида кристаллической решетки. Например, графит – мягкое вещество, алмаз – самое твердое вещество. Атомы этих веществ одинаковы, но разная кристаллическая решетка, что является причиной разных физических свойств, разного внешнего вида алмаза и графита.
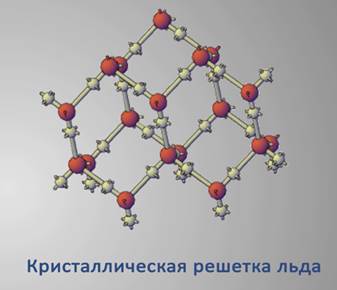
Молекулы льда расположены близко друг к другу, но кристаллическая решетка содержит пустоты, поэтому объем воды при замерзании увеличивается.
Когда идем по свежевыпавшему снегу, слышим характерный треск, вызванный разрушением кристаллических решеток снежинок.
Итак, разное расположение молекул вещества в разных агрегатных состояниях приводит к тому, что свойства твердых, жидких и газообразных веществ различны.
Важно запомнить:
1. Молекулы газа расположены на расстояниях, во много раз больше размеров самих молекул, почти не притягиваются друг к другу и движутся беспорядочно во всех направлениях. Поэтому газ не сохраняет форму и объем.
2. Расстояние между молекулами жидкости сравнимо с размерами самих молекул, притяжение между ними значительное, молекулы жидкости скачкообразно меняют свое положение, поэтому жидкости сохраняют свой объем, но меняют форму.
3. В твердых телах молекулы расположены близко друг к другу, притяжение между ними большое, поэтому твердые тела сохраняют и объем, и форму. Определенный порядок расположения молекул твердых тел называется кристаллической решеткой.
 Подпишись и будь
в курсе новых событий и новостей!
Подпишись и будь
в курсе новых событий и новостей!