

Важнейшим законом химии является закон сохранения массы веществ, который был сформулирован М.В. Ломоносовым и экспериментально доказан А.Л. Лавуазье. Современная формулировка закона следующая:
Масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции.
Из этого закона следует:
1.Число атомов каждого элемента в результате реакции должно быть одинаковым.
2.Атомы в химических реакциях не исчезают и не возникают из ничего, а в результате реакции происходит их перегруппировка с образованием новых веществ.
Закон сохранения массы вещества помогает составлять уравнения химических реакций и производить по ним расчеты.
Так запись:
H2 + O2→H2O
является лишь схемой реакции, она показывает, что водород и кислород являются реагирующими веществами, а вода – продукт реакции. Подобрав стехиометрические коэффициенты перед формулами веществ, то есть уровняв число атомов всех видов в левой и правой частях, получаем уравнение:
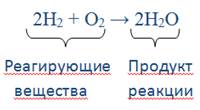
которое соответствует закону сохранения массы.
 Подпишись и будь
в курсе новых событий и новостей!
Подпишись и будь
в курсе новых событий и новостей!