В современной периодической системе Д.И. Менделеева размещено 118 химических элементов. Большая часть из них относится к металлам.
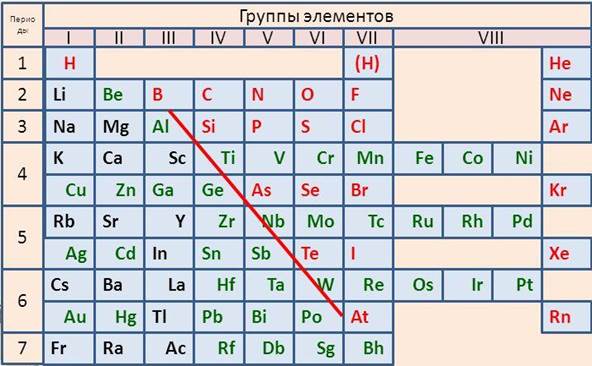
Металлы содержатся во всех группах этой системы, например, в первой группе все элементы, кроме водорода, относятся к металлам. Во второй группе - все металлы, в третьей группе все элементы являются металлами, кроме бора. В IV, V, VI группах металлы располагаются в побочных подгруппах и внизу главных подгрупп (в IV группе - это германий, олово, свинец, в V группе – сурьма, висмут, в VI группе – полоний). В VII – VIII группах металлы располагаются только в побочных подгруппах.
Таким образом, условная граница между элементами-металлами и элементами-неметаллами в главных подгруппах проходит по диагонали B (бор) - Si (кремний) – As (мышьяк) - Te (теллур) – At (астат). Все элементы побочных подгрупп относятся к металлам.
Металлы I группы главной подгруппы - литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs), франций (Fr) - называются щелочными. Их так назвали, потому что их гидроксиды являются растворимыми в воде основаниями – щелочами.
Металлы II группы главной подгруппы – магний (Mg), кальций (Ca), стронций (Sr),
барий (Ba), радий(Ra) - называются щелочноземельными. Их гидроксиды обладают щелочными свойствами, а оксиды сходны по тугоплавкости с оксидами алюминия и железа, которые ранее называли «земли».
В периодической системе выделяют группу благородных металлов: золото (Au),
серебро (Ag), платина (Pt) и металлы платиновой группы рутений (Ru), родий (Rh),
палладий (Pd), осмий (Os), иридий (Ir), их так назвали из-за блеска в изделиях и их способности не окисляться на воздухе.
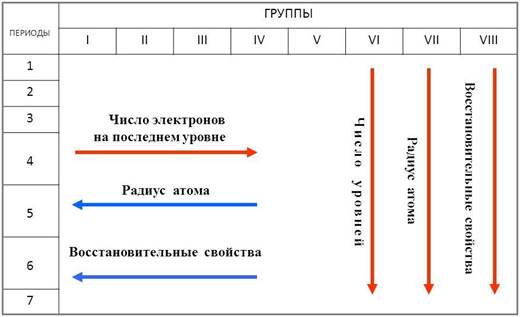
Из положения металлов в периодической системе химических элементов можно определить и особенности их строения.
Первой особенностью является небольшое число электронов на внешнем уровне
(от 1 до 3 электронов) у большинства металлов.
Ко второй особенности можно отнести сравнительно большой радиус атома.
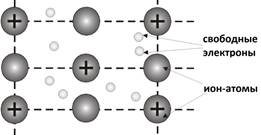
Атомы металлов в отличие от атомов неметаллов легко отдают наружные электроны и превращаются в положительно заряженные ионы. Свободные электроны перемещаются между ионами металлов. Положительные ионы металлов удерживаются все вместе за счет притяжения ко всем свободно движущимся в металлах электронам. Между этими частицами (свободными электронами и ионами металлов) возникает связь, которую называют металлической.
![]()
Схематично такую связь можно изобразить так:
; где М-символ элемента металла.
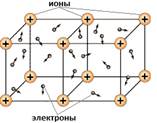
Электроны находятся в постоянном движении, при их столкновении с положительно заряженными ионами металлов ионы превращаются в нейтральные атомы, а затем снова в ионы, и такой процесс происходит непрерывно. Поэтому ввели понятие – ион-атом металла.
Металлическая связь имеется в металлах, находящихся в жидком и твердом состоянии. Твердые металлы – вещества кристаллические. Их кристаллические решетки называются металлическими. В узлах их решеток находятся ион-атомы металлов, а между ними передвигаются относительно свободные электроны. Металлическая связь является очень прочной.
В периодической системе Д.И. Менделеева из 118 химических элементов большая часть относится к металлам. Металлы содержатся во всех группах периодической системы. Они в основном расположены в левой нижней части системы, условная граница между элементами-металлами и элементами-неметаллами в главных подгруппах проходит по диагонали B (бор) - Si (кремний) – As (мышьяк) - Te (теллур) – At (астат). Все элементы побочных подгрупп относятся к металлам. Для металлов характерна металлическая химическая связь и металлическая кристаллическая решетка. Металлическая связь очень прочная.
 Подпишись и будь
в курсе новых событий и новостей!
Подпишись и будь
в курсе новых событий и новостей!